ROZDZIAŁ 7. SUPLEMENT 2
PRZYKŁAD RÓWNAŃ NEWTONA DLA MOLEKUŁY DWUATOMOWEJ
Plik pdf do wydruku: r7_supl2.pdf
Rozpatrzmy, na przykład, molekułę CO i ponumerujmy atomy: C ma nr 1, O ma nr 2. Mamy
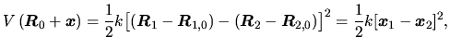
Teraz zainteresujemy się równaniami ruchu Newtona: masa razy przyspieszenie równa się siła. Składowa siły działającej na atom o masie ![]() to ujemna pochodna energii potencjalnej względem odpowiedniej współrzędnej tego atomu. Ponieważ
to ujemna pochodna energii potencjalnej względem odpowiedniej współrzędnej tego atomu. Ponieważ
![]()
![]()
![]()
![]()
![]() , więc
(kropki oznaczają pochodne po czasie):
, więc
(kropki oznaczają pochodne po czasie):
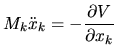 |
(1) |
dla
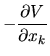 |
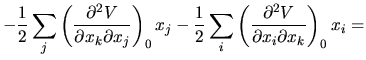 |
(2) | |
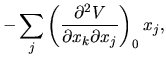 |
(3) |
przy czym skorzystaliśmy z równości pochodnych mieszanych i niezależności wyniku od indeksu sumacyjnego. W naszym przykładzie możemy teraz obliczyć siły działające na atomy. Na przykład pierwszą składową siły działającej na atom nr 1 obliczamy, różniczkując
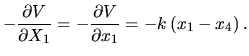
Zobaczmy, jak w naszym przykładzie wygląda macierz drugich pochodnych
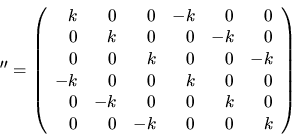 .
.
W naszym przykładzie równania Newtona mają identyczną postać. Istotnie, składowe siły, która występuje po prawej stronie równania, to wektor
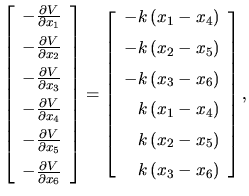 |
który jest, jak łatwo sprawdzić, korzystając ze znalezionej postaci






